Das hämostatische System verhindert signifikante Blutverluste nach Gefäßverletzungen.1 Dies erfordert eine koordiniert ablaufende Zusammenarbeit zwischen dem Gefäßendothel, den Blutplättchen sowie dem Gerinnungssystem.1,2
Im Körper besteht ein fein austariertes Gleichgewicht zwischen gerinnungsfördernden und gerinnungshemmenden Proteinen sowie zwischen fibrinolytischen (Fibrin auflösend) und antifibrinolytischen (die Fibrinauflösung hemmend) Eiweißen.1,2 Dadurch wird das Blut in einem normalen Strömungszustand gehalten.2 Nur, wenn es zu einer Verletzung gekommen ist und das Blut mit subendothelialen Strukturen (unterhalb der Gefäßinnenhaut) oder fremden Oberflächen in Kontakt kommt, wird das Gerinnungssystem aktiviert.3
Aufgaben des hämostatischen Systems sind
- die Fließfähigkeit des zirkulierenden Blutes aufrechtzuerhalten,
- Blutverlust durch Bildung von Blutgerinnseln zu verhindern,
- Gefäßverletzungen zu reparieren.1
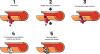
Der Wundverschluss entsteht in einem zweistufigen Prozess.1 Im ersten Schritt wird die Wunde schnell abgedichtet und die Blutung gestillt. Dieser vorläufige Gefäßverschluss, der durch Anheften und Verkleben von Thrombozyten zustande kommt, wird als primäre Hämostase bezeichnet.3
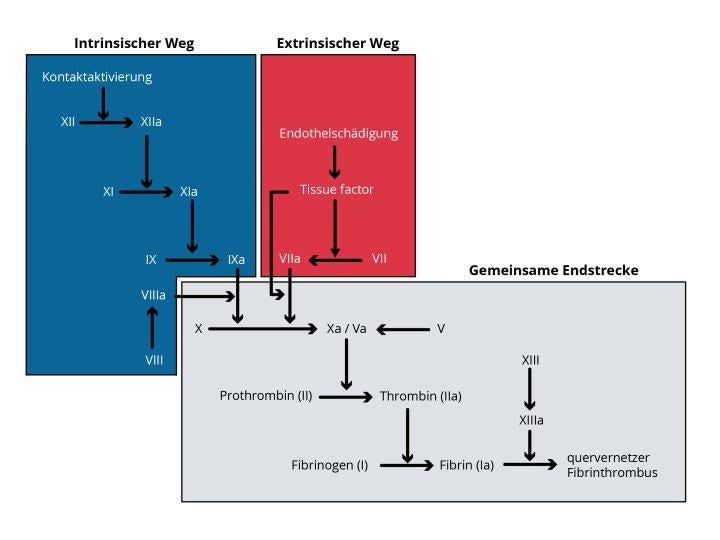
Bei der anschließenden sekundären Hämostase wird der Wundverschluss stabilisiert und die Verletzung kann abheilen.2 Die Blutgerinnung ist ein komplexes System: Unter dem Einfluss mehrerer Gerinnungsfaktoren entstehen Fibrinfasern, die die miteinander verklebten Thrombozyten zusätzlich vernetzen und stabilisieren. Später müssen die Gerinnungsfaktoren inaktiviert und das Fibrinnetz wieder aufgelöst werden (Fibrinolyse).2